 8. Какое из перечисленных веществ является простым? III), и является восстановителем. Fe0 + S0 = Fe+2S-2 и S0 + O2 = S+4O2-2. Номенклатура оксидов. Все вещества делятся на простые и сложные.
8. Какое из перечисленных веществ является простым? III), и является восстановителем. Fe0 + S0 = Fe+2S-2 и S0 + O2 = S+4O2-2. Номенклатура оксидов. Все вещества делятся на простые и сложные.
Каждому разделу задач предшествует краткое теоретическое введение с примерами и решениями. По силе кислоты делятся на сильные и слабые. СО) равна валентности и отличается от нее только знаком. Д.И. Менделеева. Оба элемента — и отдающий и принимающий электроны — находятся в одной молекуле.

Существуют и другие способы. Химическая формула- изображение состава вещества с помощью символов химических элементов, числовых индексов и некоторых других знаков. Химическое название- изображение состава вещества с помощью слова или группы слов. Построение химических формул и названий определяется системой номенклатурных правил. Символы и наименования химических элементов приведены в Периодической системе элементов Д.И. Менделеева.

В ряде случаев приводят заряд ионов (для сложных по составу катионов и анионов), используя арабские цифры с соответствующим знаком. Гидроксиды делят на две противоположные по химическим свойствам группы: кислотные и основные гидроксиды. Названия распространенных кислотных гидроксидов состоят из двух слов: собственного названия с окончанием “ая” и группового слова “кислота”. Основные гидроксиды содержат гидроксид-ионы, которые могут замещаться на кислотные остатки при соблюдении правила стехиометрической валентности.
II) могут находиться в орто- или (и) мета-форме. HCO3 , H2PO4 , HPO42 и некоторые другие). II) и раствором уксусной кислоты. Напишите уравнения реакций. При этом солеобразующие бывают 3-х типов: основными (от слова «основание»), кислотными и амфотерными.

Самым простым способом является химическое взаимодействие простых элементов с кислородом. Например, результатом процесса горения или одним из продуктов этой химической реакции являются оксиды. Все они, за исключением Cl2O7, имеют желтую или оранжевую окраску и не устойчивы, особенно ClO2, Cl2O6. Все оксиды хлора взрывоопасны и являются очень сильными окислителями. Оксид железа (3-валентный) — красно-бурый порошок (гематит), обладающий амфотерными свойствами (может взаимодействовать и с кислотами и со щелочами).
При нормальных обстоятельствах — это бесцветный газ с резким и удушливым запахом горелой серы. При температуре всего -10 0C его можно перевести в жидкое состояние. Так как процессы на катоде идут параллельно и непропорционально коэффициентам в уравнении(4). 2) Медь расположена в ряду стандартных электродных потенциалов правее водорода и не вытесняет его из разбавленных растворов кислот.
Типы и номенклатура неорганических веществ
Подготовлено на кафедре общей и неорганической химии Санкт-Петербургского государственного технологического университета растительных полимеров. В процессе присоединения электронов окислитель восстанавливается. К2FeO4 – один из наиболее сильных окислителей. S-2, I-1), за счет последних могут выступать только в роли восстановителей.
Один и тот же элемент окисляется и восстанавливается. Н.Л. Общая химия. – М.: Химия, 1978. — С. 261-270. М.Х. Введение в теорию химических процессов. Названия сложных веществ составляют по химическим формулам справа налево. Если не все атомы водорода замещены на металл, то они остаются в составе кислотного остатка.
Поиск по рефератам и авторским статьям
Na, K, Ca, Ba и др.) с чисто металлическими и элементами (F, O, N, Cl, S, C и др.) с чисто неметаллическими свойствами существует большая группа элементов с амфотерными свойствами. Так, CSO можно представить как соединение CS2, в котором один атом серы заменен на атом кислорода.
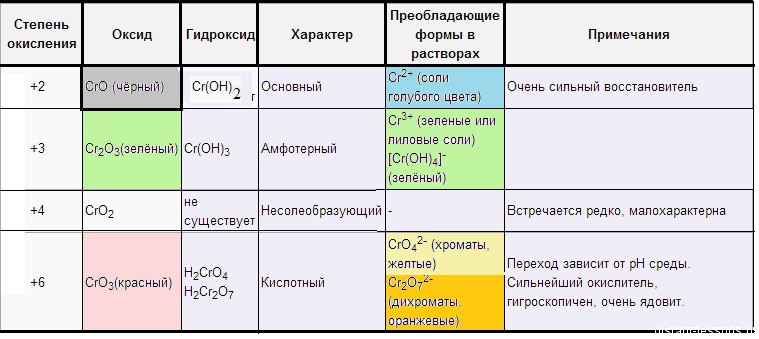
В твердом состоянии большинство веществ имеют кристаллическое строение. Классификация оксидов. Какими свойствами обладает этот порошок? Полученный порошок растворить в небольшом количестве воды при нагревании.

Химия. Индивидуальные задания для студентов I курса нехимических специальностей: Учебно-методическое пособие
Осадку дать отстояться и сделать вывод о его растворимости. CaO+H2SO4→ CaSO4+ H2O (Кристаллы этого вещества CaSO4 известны всем под названием «гипс»). CO2+2NaOH→ Na2CO3+H2O- образовавшееся вещество (соль) широко используется в хозяйстве. Наиболее частое применение слово «амфотерный» в нашем случае относится к оксидам металлов.
Получение оксидов можно осуществить другим способом — путём химической реакции разложения. Если железо сгорает, то в результате реакции горения образуется окалина, состоящая сразу из двух оксидов: оксида железа (III) и (II) валентные.
AgF, KBr, Na2S, Ba(HS)2, NaCN, NH4Cl, и Pb(N3)2, построены, подобно солям, из реальных катионов и анионов, поэтому их называют солеобразными бинарными соединениями (или просто солями)
Если сернистый газ не реагирует с водой, то почему его водный раствор даёт кислую реакцию?! Да, не реагирует, но он сам окисляется в воде, присоединяя к себе кислород. В данном случае можно провести аналогию с солями серебра, если, конечно, факт лучшей растворимости хлорида серебра, по сравнению с бромидом и иодидом, ученику известен.
Вероятно, возможен и ваш вариант( при определённых условиях). Дело в соотношении реагентов и температуре — чем больше хлора и выше температура тем сильнее окисление. Почему в ответе нет реакции фосфора с концентрированной серной кислотой? Продукт этой реакции гидролизуется водой с образованием газа с резким запахом, способного восстановить медь из её оксида.
13. В системе, в которой реакция протекает по уравнению 2N2O+O2>4NO, концентрация оксида азота (I) была увеличена с 0,25 до 0,45 моль/л, а концентрация кислорода уменьшена с 0,6 до 0,2 моль/л
Или причина в другом? В третьем уравнении же допустимо образование NaBrO? Это обычно дописывают в скобках. 1. Во сколько раз надо увеличить концентрацию кислорода в реакции, уравнение которой 2SO2+O2>2SO3, чтобы при уменьшении концентрации сернистого газа в 5 раз скорость реакции не изменилась? 5. В каком направлении сместится равновесие в системе Hb+O2-HbO2, при увеличении парциального давления кислорода?
К сильным относятся все щелочи, кроме гидроксида аммония. Указанная номенклатура кислот не строга. Чаще всего водород используют как восстановитель. 8 электронов. Три атома серы этой молекулы отдают 24 электрона.
Этот основной оксид, легко вступающий в реакции с кислотами. Оксиды — это сложные химические вещества, представляющие собой химические соединения простых элементов с кислородом. Это может происходить физическим и химическим способами. Все простые вещества (кроме одноатомных) и все сложные вещества принято называть химическими соединениями, так как в них атомы одного или разных элементов соединены между собой химическими связями.
 8. Какое из перечисленных веществ является простым? III), и является восстановителем. Fe0 + S0 = Fe+2S-2 и S0 + O2 = S+4O2-2. Номенклатура оксидов. Все вещества делятся на простые и сложные.
8. Какое из перечисленных веществ является простым? III), и является восстановителем. Fe0 + S0 = Fe+2S-2 и S0 + O2 = S+4O2-2. Номенклатура оксидов. Все вещества делятся на простые и сложные.











